КЛИНИЧЕСКИЙ СЛУЧАЙ
Ребенок с антибиотик-ассоциированной диареей
ПМ-RX-2025-02-023

- Внедрение антибиотиков в педиатрическую практику позволило кардинально решить проблему снижения заболеваемости и смертности от инфекционной патологии. Однако их широкое и, нередко, необоснованное применение приводит к осложнениям, среди которых особое место занимает нарушение микроэкологии желудочно-кишечного тракта человека [1].
- ААД (антибиотик-ассоциированная диарея) — это три и более эпизодов неоформленного стула в течение двух или более последовательных дней, которые появляются на фоне применения антибактериальных средств или в течение 8 недель после их отмены при отсутствии других причин [2].
- В литературных источниках отмечается большой разброс данных относительно частоты АДД в детской популяции. В проведенных ранее исследованиях этот показатель колебался в пределах 11–40%, но сохранялся стабильно высоким на протяжении последних десятилетий [3, 4].
- 1. Нижевич А.А., Ахмадеева Э. Н., Амирова В. Р. Антибиотик-ассоциированная диарея у детей // ПМ. 2009. №39.
- 2. ВОЗ: Лечение диареи, 2006.
- 3. Turck D., Bernet J.P., Marx J. et al. Incidence and risk factors of oral antibiotic-associated diarrhea in an outpatient pediatric population. J Pediatr Gastroenterol Nutr. 2003; 37: 22–6.
- 4. Elstner C.L., Lindsay A.N., Book L.S., Matsen J.M. Lack of relationship of Clostridium difficile to antibiotic-associated diarrhea in children.PediatrInfDis. 1983; 2: 364–6.
ПМ-RX-2025-02-023
Какой из перечисленных факторов НЕ влияет на развитие ААД?
Выберите один вариант ответа
Правильный ответ:

Факторы риска развития диареи, ассоциированной с приемом антибиотиков
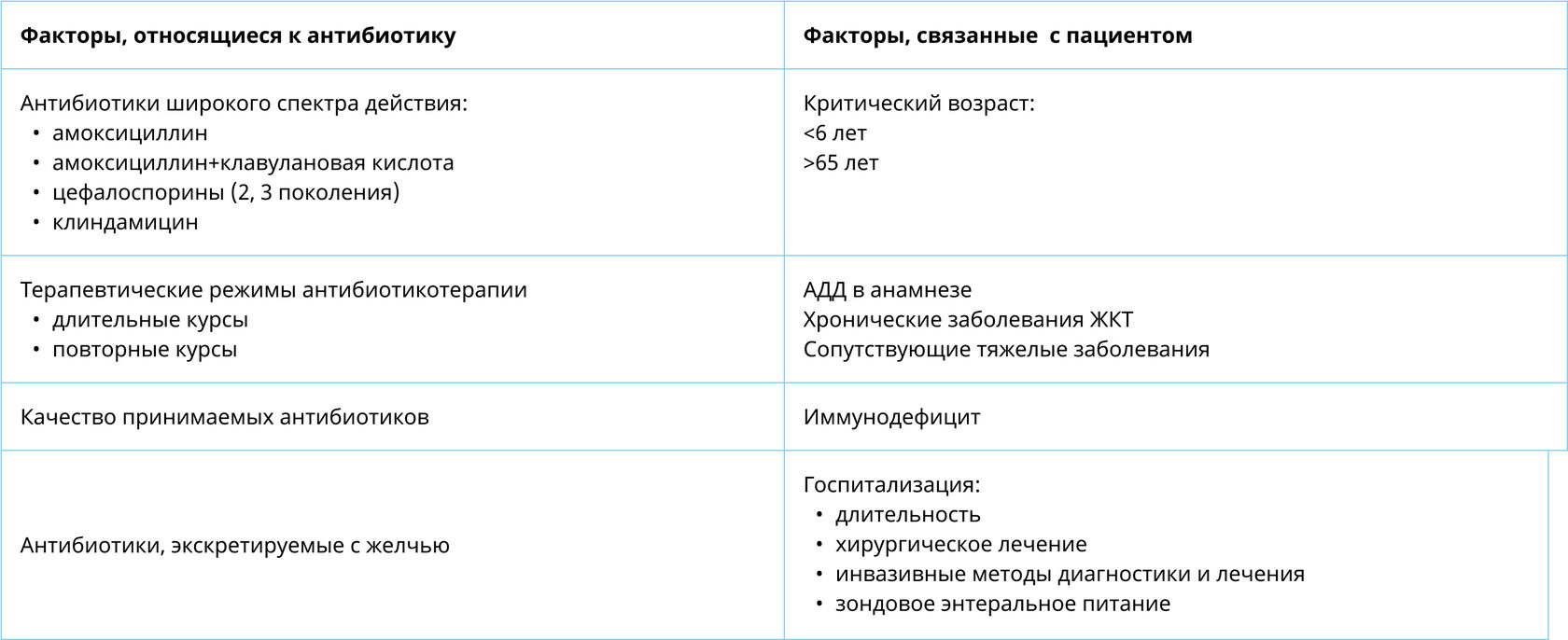
- McFarland L.V. Facteurs de risque de la diarrhea associee aux antibiotiques.Une revue de la litterature. AnnMed Interne, 1998; 149:261–6.
ПМ-RX-2025-02-023
Механизмы развития диареи на фоне применения АБ
- Clostridioides difficile (10-20%)
- Staphylococcus aureus
- Salmonella spp.
- Clostridium perfringens
- Klebsiella oxytoca
- Грибы рода Candida
- Усиление моторики кишечника (эритромицин)
- Токсическое воздействие на структуру кишечного эпителия (неомицин, канамицин)
- Воздействие на кишечный кровоток (пенициллин, сульфаниламиды)
- Захарова И. Н., Бережная И. В., Сугян Н. Г. Антибиотик-ассоциированные диареи у детей: что нового? // МС. 2017. №19.
Каскад патологических реакций вследствие нарушения слизистой оболочки кишечника при антибиотикотерапии
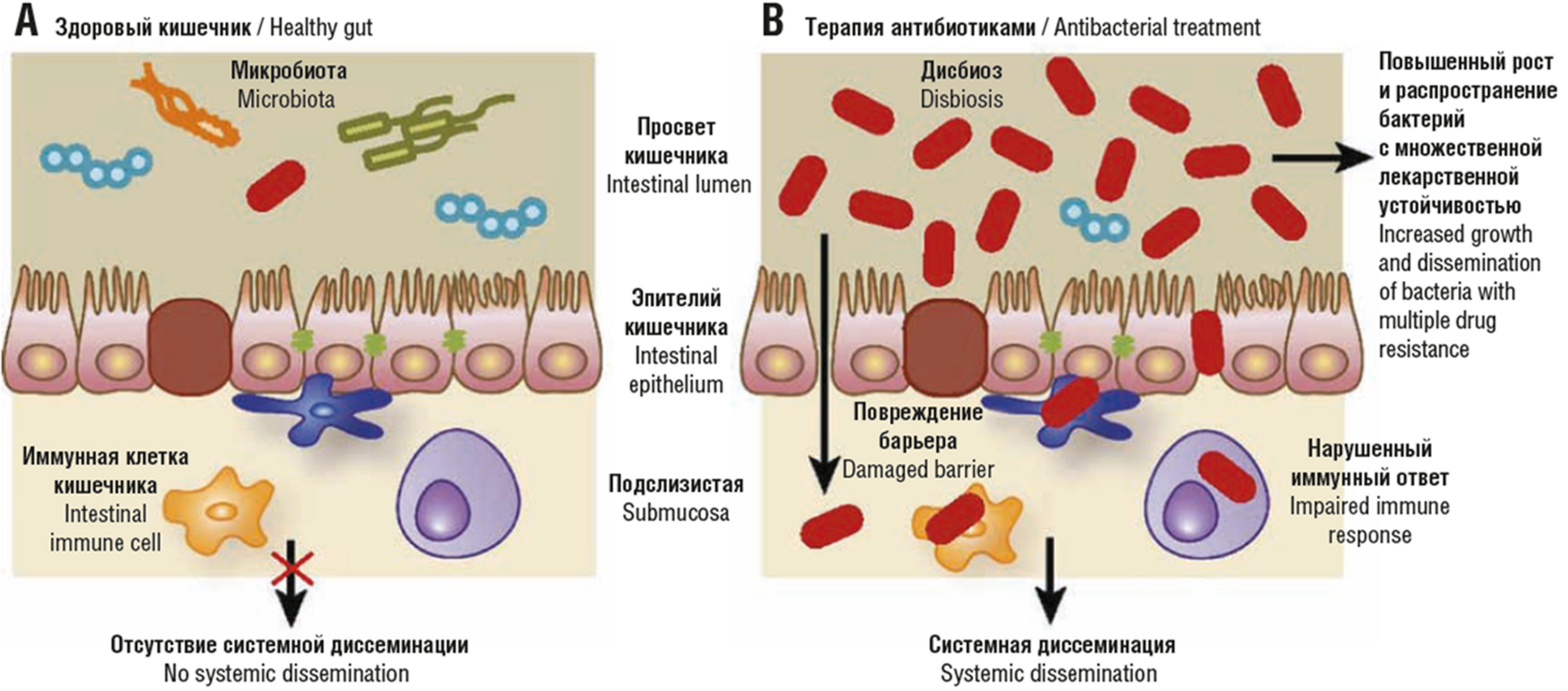
- Klemm E.J., Wong V.K., Dougan G. Emergence of dominant multidrug-resistant bacterial clades: Lessons from history and whole-genome sequencing. Proc Natl Acad Sci U S A. 2018;115(51):12872–12877. DOI: 10.1073/pnas.1717162115.
Практически любой антибактериальный препарат может вызвать ААД, но чаще она развивается при приеме клиндамицина (20–30%), амоксициллина/клавуланата (10–25%), цефалоспоринов 2–3-го поколения (9–25,8%), эритромицина (11–1%), кларитромицина и ампициллина (5–10%).
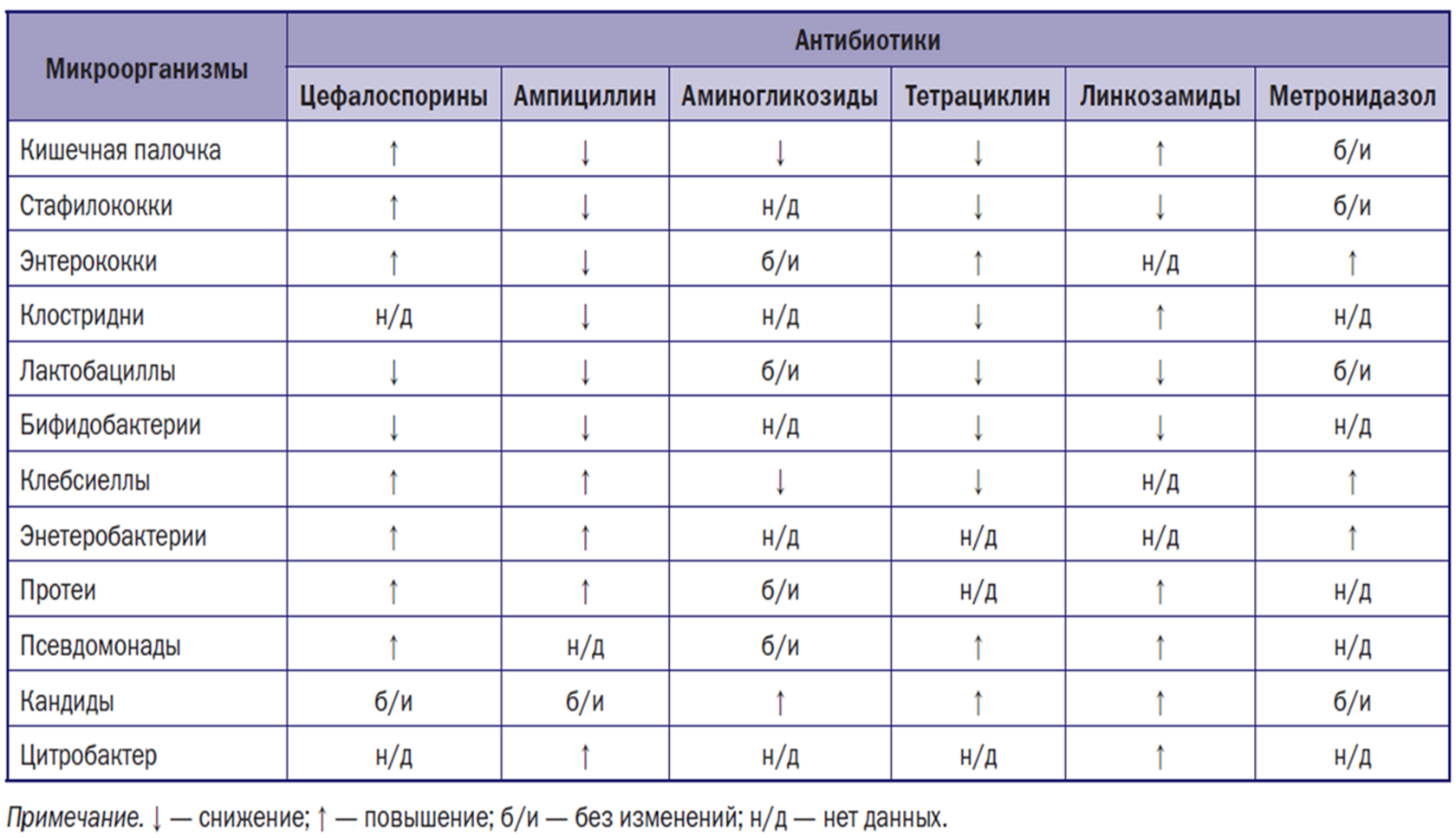
- Запруднов А.М., Мазанкова Л.Н. Микробная флора кишечника и пробиотики. М.: Педиатрия. 1999. 48 с.
Действие антибактериальных препаратов на состав микробной флоры толстой кишки
- Собственные побочные эффекты АБ (например, усиление перистальтики кишечника при приеме амоксициллина с клавулановой кислотой, макролидов, которые обладают мотилиноподобным действием на рецепторы кишечника) [1].
- Осмотическая диарея в результате нарушения метаболизма желчных кислот и углеводов в кишечнике (например, при приеме фосфомицина трометамола) [2].
- Избыточный рост бактерий в результате подавления облигатной интестинальной микрофлоры кишечника [3].
- 1. Hogenauer C., Hammer H.F., Krejs G.J., Reisinger E.C. Mechanisms and management of antibiot icssociated diarrhea. Clin Infect Dis, 1998, 27: 702-710.
- 2. Захарова И.Н., Дмитриева Ю.А. Антибиотикоассоциированные диареи: лечение и профилактика. Consiliummedicum. Педиатрия, 2009, 2: 7-10.
- 3. Hempel S., Newberry S.J., Maher A.R. et al. Probiotics for the Prevention and Treatment of Antibiotic-Associated Diarrhea. A Systematic Review and Meta-analysis. JAMA, 2012 May 9, 307(18).
ПМ-RX-2025-02-023
Анамнез заболевания:
Мальчик, 5 лет, 15 октября 2023 года направлен педиатром к гастроэнтерологу с жалобами на:
- незначительное повышение температуры — до 37,2 °C;
- снижение аппетита;
- вздутие живота;
- умеренные боли в животе в области пупка;
- частый (до 5–6 раз в день) водянистый стул.
С 1 октября 2023 года принимал антибиотики (амоксициллин) по поводу ОРИ с подозрением на острый средний отит, назначенные врачом. На 5-й день после начала лечения (5 октября) у ребенка началась диарея, которая постепенно усиливалась. В течение нескольких дней наблюдались также боли в животе и снижение аппетита. Родители связывают начало диареи с приемом антибиотиков.
За последние 6 месяцев это уже третий курс антибиотикотерапии. Ранее был прием (амоксициллины, цефалоспорины) по поводу острого бронхита, риносинусита. Курсы — 14 дней, пробиотики не назначались.
Из анамнеза жизни:
- Ребенок от первой беременности, которая протекала без осложнений, инфекций во время беременности не было. Роды естественные, в срок (на 40-й неделе). Масса при рождении: 3800 г, рост: 52 см. Оценка по шкале Апгар: 8–9 баллов.
- В период новорожденности проблем не было, выписан из роддома на 5-й день. Состояние здоровья в норме. Физическое развитие согласно возрасту.
- Вакцинирован согласно национальному календарю, все прививки сделаны в срок.
- ОРВИ — 2–3 раза в год. В последние 6 месяцев — острый бронхит, острый средний отит, острый риносинусит.
- Аллергии нет.
- Семейный анамнез: родители здоровы, хронических и наследственных заболеваний нет.
- Социальные условия: ребенок живет с обоими родителями в квартире. Посещает детский сад, общается с детьми. Активный, общительный, любит играть с детьми. Занимается рисованием и конструированием.
- Контакт с инфекционными больными отрицает.
При осмотре:
- Состояние удовлетворительное, сознание ясное, адекватно реагирует на обращения. Температура тела: 37,0 °C.
- Нормостеник, масса тела и рост в пределах возрастной нормы.
- Кожа нормальной окраски, сухая, тургор умеренно снижен. Высыпаний нет.
- ЧСС 100 уд/мин, ритмичный, без шумов. АД 90/60 мм рт. ст., в пределах возрастной нормы. ЧД 22 в минуту, ритмичное, без затруднений.
- Аускультация легких: дыхание везикулярное, без хрипов.
- Рефлексы в пределах нормы, мышечный тонус не нарушен, координация движений сохранена.
- Отмечается умеренное вздутие живота, болезненность при пальпации в области пупка. Перистальтика усилена. Стул до 5–6 раз в сутки, водянистый, без примесей крови.
- Мочеиспускание в норме, диурез снижен.
ПМ-RX-2025-02-023
Какова основная клиническая характеристика антибиотик-ассоциированной диареи?
Выберите один вариант ответа
Правильный ответ:

ПМ-RX-2025-02-023
Какой из патогенов чаще всего ассоциируется с антибиотик-ассоциированной диареей у детей?
Выберите один вариант ответа
Правильный ответ:

ПМ-RX-2025-02-023
Критерии тяжести ААД
Клинические симптомы появляются на фоне антибиотикотерапии или в течение 6–8 нед. после ее окончания
Легкое течение
- Водянистая диарея до 5–7 р/сут
- Умеренная боль в животе
- Отсутствие лихорадки и лейкоцитоза
Среднетяжелое течение
- Водянистая диарея 10–15 р/сут
- Боль в животе
- Лихорадка до 38 °C
- Умеренная дегидратация
- Лейкоцитоз
Тяжелое течение
Псевдомембранозный колит
- Диарея 15–20 р/сут (примесь крови в кале)
- Астенизация
- Лихорадка 38-40 °C
- Тяжелая дегидратация
- Высокий лейкоцитоз
- Корнеева О.Н., Ивашкин В.Т. Антибиотикоассоциированный колит: патоморфология, клиника, лечение // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. – 2007. – № 3. – С. 65-69.
ПМ-RX-2025-02-023
Лабораторные и инструментальные данные:
- лейкоциты — 8,5 × 109/л
- гемоглобин — 120 г/л
- тромбоциты — 250 × 109/л
- СОЭ — 15 мм/ч
- глюкоза: 4,1 ммоль/л
- уровень электролитов: натрий — 135 ммоль/л (норма 135–145)
- калий — 3,5 ммоль/л (норма 3,5–5,0)
- хлор — 100 ммоль/л (норма 98–106)
- Уровень креатинина и мочевины в пределах нормы.
- отрицательный результат
- цвет соломенно-желтый, прозрачная
- реакция мочи — кислая
- относительная плотность — 1,013
- белок отриц.
- лейкоциты — 0–1 в поле зрения
- эпителий плоский — 0–1 в поле зрения
- водянистый стул
- присутствие мышечных волокон
- без патологических примесей
- без патологии
K52.9 Неинфекционный гастроэнтерит и колит неуточненный.
Легкая степень обезвоживания.
Ошибки в тактике ведения пациента:
1. Длительный и нерациональный курс антибиотиков:
- Ребенку при ОРИ назначались антибиотики без должного обоснования, что способствовало развитию дисбиоза и, как следствие, ААД.
- Не проводился анализ на чувствительность микроорганизмов, что могло предотвратить назначение ненужных антибиотиков.
2. Отсутствие профилактики ААД:
- Не было рекомендовано использование пробиотиков во время или после курса антибиотиков, что могло бы снизить риск развития диареи.
ПМ-RX-2025-02-023
Долгосрочные последствия антибиотик-ассоциированного дисбиоза: скрытая часть айсберга
Нарушение микробиоты кишечника под действием антибиотиков повышает риск хронических заболеваний из-за локального и системного усиления воспалительных реакций, которое приводит к нарушению регуляции метаболизма и иммунного гомеостаза.
Видимая часть айсберга — краткосрочные последствия:
- Диарея
(до 6 недель после приема антибиотиков) - C. difficile-ассоциированные заболевания
- Candida
Скрытая часть айсберга — долгосрочные последствия:
- Воспалительное заболевание кишечника
- Нарушение обмена веществ
- Ожирение
- Аллергия
- Астма
- Сахарный диабет
- Тревожность

Долгосрочные последствия антибиотик-ассоциированного дисбиоза: скрытая часть айсберга
Перинатальный период, характеризующийся развитием иммунной системы наряду с созреванием кишечной микробиоты, оказывается особенно чувствительным этапом, в течение которого антибиотик-ассоциированный дисбиоз приводит к более высокому риску заболеваний в более позднем возрасте.
- Воспалительные заболевания кишечника
Болезнь Крона - Нарушение обмена веществ
Сахарный диабет, ожирение - Атопические заболевания
Бронхиальная астма - Аллергия
- Тревожность и депрессия

- Francino M.P. Antibiotics and the Human Gut Microbiome: Dysbiosis and Accumulation of Resistances. Front Microbiol. 2016;6:1543.
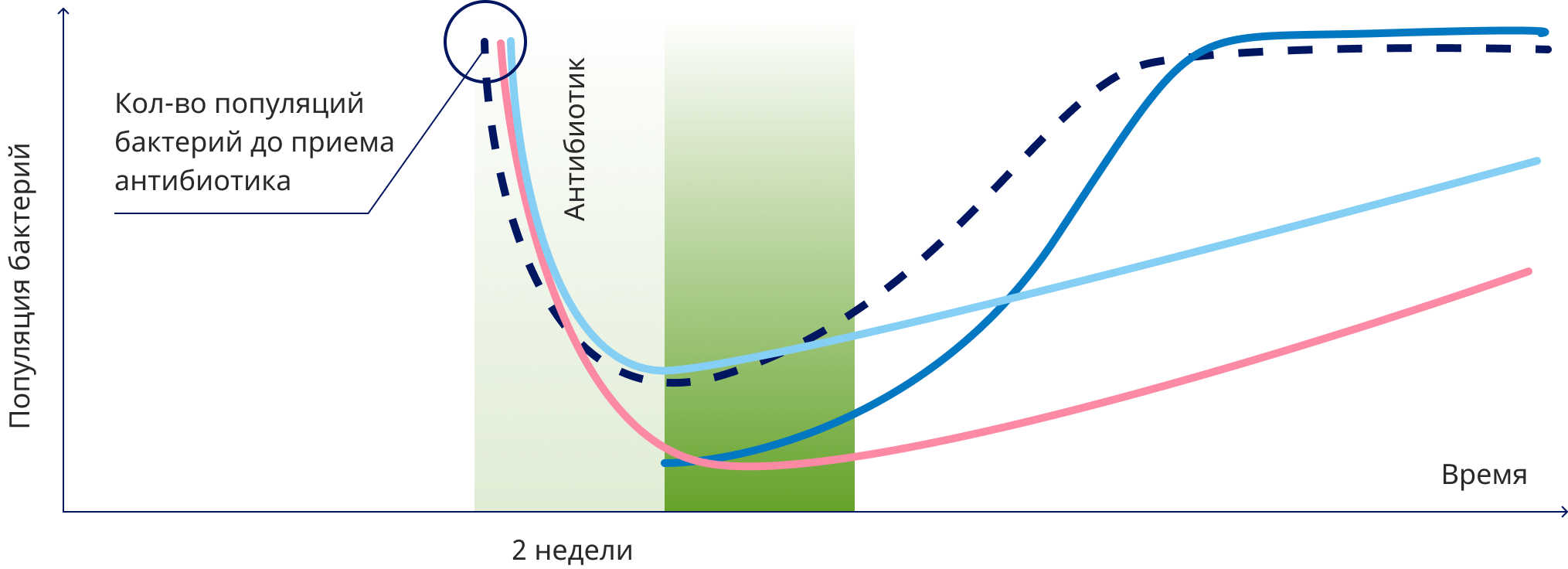
Исследование Swidsinski:
как защитить собственную уникальную микробиоту?

Двухнедельное лечение антибиотиками вызывает уменьшение доминирующих бактериальных популяций микробиоты;

Применение S. boulardii CNCM I-745 во время лечения антибиотиками минимизирует внезапное уменьшение бактериальных популяций;

Когда S. boulardii CNCM I-745 вводится после лечения антибиотиками, восстановление микробиоты ускоряется до исходного уровня;

Оптимальное использование S. boulardii CNCM I-745: во время и после лечения антибиотиками в течение 2 недель
ПМ-RX-2025-02-023
В пользу какого пробиотика следует сделать выбор при лечении ААД?
Выберите один вариант ответа
Правильный ответ:

ПМ-RX-2025-02-023
Почему Энтерол®?

ЭНТЕРОЛ® — это оригинальный2 лекарственный препарат на основе Saccharomyces boulardii CNCM I-745®, который производится во Франции. Аналогов в России нет.


ПЕРВООТКРЫВАТЕЛИ ПРОБИОТИКОВ

Уникальны2, как отпечаток пальца
- Род: Saccharomyces
- Вид: boulardii
- Наименование штамма: CNCM I-745

Сахаромицеты буларди CNCM I-745
- Микроорганизм хранится в международных органах по депонированию микроорганизмов в институте Пастера во Франции
- 1. Данные о назначениях гастроэнтерологов и педиатров при диагнозе «кишечные инфекции (А00-А09)» в 4 кв. 2022г., согласно исследованию PrindexTM «Мониторинг назначений врачей», проведенному ООО «Ипсос Комкон» в 17 городах РФ.
- 2. https://www.saccharomycesboulardii.com/
Энтерол® — уникальный небактериальный пробиотик для любого антибиотика и универсальное противодиарейное средство


Обладает естественной устойчивостью к антибиотикам

Возможен одновременный прием с пероральными антибиотиками

Курс лечения соответствует курсу применения антибиотика

Исключает риск передачи генов антибиотикорезистентности и сокращает количество таких генов
- 1. Энтерол® — единственный лекарственный препарат на основе Сахаромицет буларди согласно ГРЛС на дату 18.01.2025.
- 2. ИМП лекарственного препарата Энтерол®.
- 3. Cifuentes S.G., Prado M.B., Fornasini M., Cohen H., Baldeón M.E., Cárdenas P.A. Добавка Saccharomyces boulardii CNCM I-745 изменяет фекальный резистом во время эрадикационной терапии Helicobacter pylori. Хеликобактер. 2022 апрель; 27 (2): e12870. doi: 10.1111/hel.12870. Epub 2022, 6 января. PMID: 34990038.
Исследование Neut K. 2017:
одновременный прием небактериального пробиотика Saccharomyces boulardii CNCM I-745 (препарат Энтерол®) совместно с пероральными антибиотиками: профилактика без риска снижения эффективности пробиотика
- В отличие от S. boulardii ни один из пробиотиков бактериального происхождения не был резистентен ко всем испытуемым антибиотикам.
- У 8 наиболее часто используемых антибиотиков (амоксициллин, амоксициллин + клавулановая кислота, цефуроксим, азитромицин, кларитромицин, пристинамицин, ципрофлоксацин и левофлоксацин) чувствительность к бактериальному пробиотику возникает в 75% случаев.
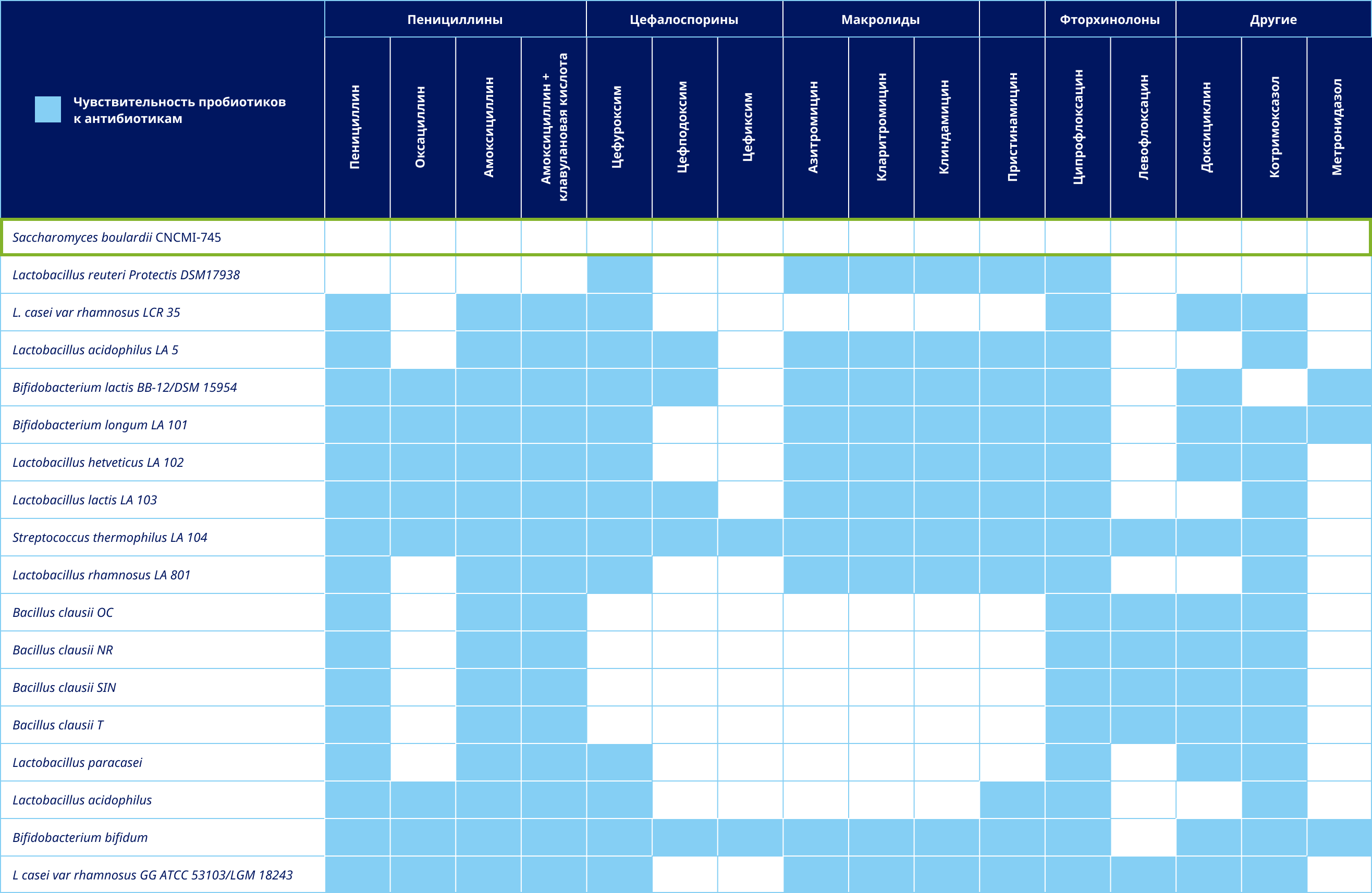
- Неут К., Мэхиукс С. и др. Чувствительность к антибиотикам пробиотических штаммов: разумно ли комбинировать пробиотики с антибиотиками? Med Mal Infect. 2017 Nov;47(7):477-483. doi: 10.1016/j.medmal.2017.07.001. Epub 2017 Aug 7.
Небактериальный пробиотик Saccharomyces boulardii CNCM I-745 (препарат Энтерол®) имеет сходные в сравнении с бактериальными пробиотиками механизмы действия, но обладают рядом уникальных преимуществ
Saccharomyces boulardii CNCM I-745
- Благодаря таким свойствам, как крупный размер клетки, а также способности к выработке антимикробных пептидов, SB успешно конкурируют с патогенной флорой1
- Создают благоприятные условия для восстановления нормальной микробиоты благодаря способности продуцировать пребиотические вещества1
- SB способны восстанавливать барьерную функцию кишечного эпителия путем прямого воздействия на энтероциты, обеспечивая их регенерацию и восстанавливая их ферментативную активность1
Преимущества:
- SB можно применять вместе с любым антибиотиком, так как они обладают естественной резистентностью к АБ1,2
- При попадании в ЖКТ выживаемость SB составляет 100%1
- SB не несут опасности передачи генов антибиотикорезистентности патогенным бактериям1,2
Бактериальные пробиотики
- Вытеснение патогенной флоры благодаря способности синтезировать бактерицидные вещества (молочную кислоту, КЦЖК, перекись водорода, сероводород)4
- Синтезируют молочную кислоту, лактозу, аминокислоты и жирные кислоты, которые способствуют восстановлению в кишечнике биологической среды для нормальной микробиоты5
- Лакто- и бифидобактерии способны синтезировать факторы роста, муцин, полиамины, усиливающие процессы регенерации эпителия и укрепляющие цитоскелет энтероцитов4
Минусы:
- Одновременный прием бактериальных пробиотиков с антибиотиками не вполне обоснован, поскольку АБ могут подавлять активность бактерий6
- При попадании в ЖКТ бактериальные пробиотики полностью не устойчивы к его агрессивным средам3
- Существует опасность передачи генов антибиотикорезистентности от пробиотических бактерий другим микроорганизмам, населяющим кишечник7
- 1. Pais P, Almeida V, Yılmaz M, Teixeira MC. Saccharomyces boulardii: What Makes It Tick as Successful Probiotic? J Fungi (Basel). 2020 Jun 4;6(2):78. doi: 10.3390/jof6020078. PMID: 32512834; PMCID: PMC7344949.
- 2. McFarland LV. Systematic review and meta-analysis of Saccharomyces boulardii in adult patients. World J Gastroenterol. 2010 May 14;16(18):2202-22. doi: 10.3748/wjg.v16.i18.2202. PMID: 20458757; PMCID: PMC2868213.
- 3. Madsen K. I. The use ofprobiotics in gastrointestinal disease // Can. J. Gastroenterol. — 2001. — V. 15. — S. 12. — P. 817—22.
- 4. Е. А. Корниенко Современные принципы выбора пробиотиков «Детские инфекции» 2007, № 3, с. 64-69
- 5. Скворцов В.В., Меднова Д.А., Халилова У.А. МИКОБИОТА КИШЕЧНИКА // Медицинская сестра. 2016. №6.
- 6. Белоусова О.Ю. Пробиотики при антибиотик-ассоциированной диарее у детей: обоснованный выбор // ЗР. 2016. №5 (73).
- 7. Кайбышева В.О., Никонов Е.Л. Пробиотики с позиции доказательной медицины. Доказательная гастроэнтерология. 2019;8(3):45-54
Практические рекомендации РГА и НСОИМ: Saccharomyces boulardii CNCM I-745 у детей

- 1. Ивашкин В.Т., Горелов А.В., Абдулганиева Д.И., Алексеева О.П., Алексеенко С.А., Барановский А.Ю., Захарова И.Н., Зольникова О.Ю., Ивашкин К.В., Ивашкина Н.Ю., Корочанская Н.В., Маммаев С.Н., Николаева С.В., Полуэктова Е.А., Трухманов А.С., Усенко Д.В., Хлынов И.Б., Цуканов В.В., Шифрин О.С., Бережная И.В., Лапина Т.Л., Масленников Р.В., Сугян Н.Г., Ульянин А.И. Методические рекомендации Научного сообщества по содействию клиническому изучению микробиома человека (НСОИМ) и Российской гастроэнтерологической ассоциации (РГА) по применению пробиотиков, пребиотиков, синбиотиков, метабиотиков и обогащенных ими функциональных пищевых продуктов для лечения и профилактики заболеваний гастроэнтерологического профиля у взрослых и детей. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2024. https:// doi.org/10.22416/1382-4376-2024-117-312
WGO: Saccharomyces boulardii CNCM I-745 для профилактики ААД у детей и взрослых с уровнем доказательности 1

ESPGHAN: Saccharomyces boulardii CNCM I-745 для профилактики ААД у детей

- Если рассматривается использование пробиотиков для профилактики ААД у детей
- Рабочая группа ESPGHAN рекомендует применение S. boulardii для профилактики ААД у детей
- 1. Szajewska, Hania MD*; Berni Canani, Roberto MD†; Domellöf, Magnus MD‡; Guarino, Alfredo MD†; Hojsak, Iva MD§; Indrio, Flavia MD‖; Lo Vecchio, Andrea MD†; Mihatsch, Walter A. MD¶; Mosca, Alexis MD#; Orel, Rok MD**; Salvatore, Silvia MD††; Shamir, Raanan MD‡‡; van den Akker, Chris H. P. MD§§; van Goudoever, Johannes B. MD§§; Vandenplas, Yvan MD‖‖; Weizman, Zvi MD¶¶; on behalf of the ESPGHAN Special Interest Group on Gut Microbiota and Modifications. Probiotics for the Management of Pediatric Gastrointestinal Disorders: Position Paper of the ESPGHAN Special Interest Group on Gut Microbiota and Modifications. Journal of Pediatric Gastroenterology and Nutrition 76(2):p 232-247, February 2023.
Резолюция Совета подтвердила необходимость строгого контроля над защитой микробиоты ребенка при приеме антибиотиков

Ознакомиться с полным текстом Резолюции можно здесь:
https://www.biocodex-academy.ru/page28688611.htmlШтамм Saccharomyces boulardii CNCM I-745® вошел в Резолюцию Совета благодаря соответствию требованиям Совета к пробиотикам

Обладает клинически доказанной эффективностью и безопасностью применения

В отличие от бактериальных пробиотиков, обладает естественной устойчивостью к антибиотикам, поэтому может применяться совместно с антибиотиками

Содержит жизнеспособные сахаромицеты буларди
- 1. ИМП лекарственного препарата Энтерол®
Лечение ААД

- Захарова И.Н., Бережная И.В., Сугян Н.Г. Антибиотик-ассоциированные диареи у детей: что нового? // МС. 2017. №19.
ПМ-RX-2025-02-023
Ребенку проводилась следующая терапия:
- Диета: легкая, с высоким содержанием углеводов, ограничение жиров и клетчатки.
- ОРС (оральные регидратационные растворы) для восполнения водно-электролитного баланса. Регидрон или аналогичные растворы: в первые 4–6 часов — 50–100 мл на каждый кг массы тела (маленькими порциями по 5–10 мл каждые 5–10 мин.), далее — в умеренных количествах до восстановления аппетита и улучшения общего состояния.
- Энтерол® 1 пакетик (250 мг) 2 раза в сутки.
- Наблюдение за состоянием ребенка, контроль уровня гидратации, частоты стула, температуры тела.
- Родителям даны рекомендации по уходу за ребенком и наблюдению за состоянием. Объяснено значение пробиотиков и важность соблюдения диеты.
Энтерол® саше — форма выпуска, созданная специально для детей

УДОБНАЯ ФОРМА ПРИЕМА ПРЕПАРАТА

ПРИЯТНЫЙ ВКУС
Содержимое пакетика можно размешать с водой или другим напитком, а также добавить в пищу или в бутылочку с детским питанием непосредственно перед приемом.


- ИМП лекарственного препарата Энтерол®
Результаты лечения
- На третий день лечения состояние ребенка значительно улучшилось: стул стал менее частым (2–3 раза в день), исчезли боли в животе, температура нормализовалась. Обезвоживание было полностью устранено.
- Через 10 дней после начала терапии — частота стула уменьшилась до 1–2 раз в день, исчезли боли и вздутие живота.
Данный клинический случай подчеркивает важность рационального назначения антибиотиков, а также необходимость использования пробиотиков для профилактики и лечения ААД.
Курс лечения по дням соответствует курсу применения антибиотика.
ПМ-RX-2025-02-023

Уважаемый коллега, благодарим за прохождение клинического случая!
ПМ-RX-2025-02-023




